Слайд 1Описание слайда:
Хондропротекторы Сделал : Ергешов С. С. Проверила : Карина К. К.
Слайд 2Описание слайда:
При помощи матрикса осуществляется снабжение хондроцитов питанием, водой, кислородом: при движении под действием веса тела суставной хрящ нижних конечностей сдавливается, как губка, а неиспользованная тканевая жидкость выдавливается из него. При разгрузке, давление в хряще падает, и хрящ, аналогично губке, расширяясь, всасывает в себя свежую, богатую питательными веществами тканевую жидкость. При каждом шаге осуществляется питание хряща.
Слайд 3Слайд 4Слайд 5Описание слайда:
На что направлена хондропротективная терапия? Стимуляция хондроцитов Снижение активности лизосомальных ферментов Увеличение резистентности хондроцитов к воздействию провоспалительных цитокинов Увеличение резистентности матрикса хряща к воздействию НПВП Активация анаболических процессов в матриксе хряща Создание предпосылок для формирования устойчивого хряща
Слайд 6Слайд 7Описание слайда:
Препараты, модифицирующие течение остеоартроза. Глюкозамина сульфат (Дона) – назначается в виде порошка в дозе 1500 мг раз в сутки. Для оказания симптоматического действия достаточно приема препарата в течение 6-12 недель. Для оказания базисного действия необходимо принимать длительно.
Курс 2-3 раза в год. Схема введения ампулированной формы препрата для внутримышечных инъекций : 2-3 раза в неделю. Хондроитин-6 сульфат (Структум, Хондроитин-АКОС) Принимается в дозе 500 мг 2 раза вдень минимум 6 недель для достижения симптоматического эффекта.
Оптимальный курс 3-6 месяцев, последействие 3-5 месяцев.
Слайд 8Описание слайда:
Препараты, модифицирующие течение остеоартроза. 3. Комбинированные препараты: в одной лекарственной форме глюкозамина сульфат (или глюкозамина хлорид) и хондроитин-6-сульфат. ( Хондро, Артра и Терафлекс). Курс лечения 4-6 месяцев.
Хондроитин сульфат и глюкозамин сульфат — гликозоаминогликаны , расположенные в матриксе суставного хряща. В настоящее время имеется большая доказательная база их эффективности . Наиболее выраженный и длительный эффект обеспечивает комбинация этих препаратов.
Через три года лечения не выявляется значимого сужения суставной щели в отличие от пациентов, не получающих хондропротекторов.
Слайд 9Описание слайда:
Симптоматические компоненты замедленного действия Хондроитин участвует в построении хрящевой ткани снижает активность ферментов, разрушающих суставной хрящ уменьшает болевой синдром в суставах
Слайд 10Описание слайда:
Структурно-модифицирующие свойства глюкозамина Глюкозамин сульфат (1500 мг/день) замедляет прогрессирование остеоартроза коленного сустава [1,2] В группе плацебо выраженное сужение суставной щели (>0.5 мм) через 3 года
Слайд 11Описание слайда:
Структурно-модифицирующие свойства хондроитина Хондроитин сульфата замедляет сужение суставной щели при остеоартрозе коленного сустава В группе плацебо сужение минимальной ширины суставной щели через 2 года
Слайд 12Описание слайда:
Синергизм глюкозамина и хондроитина
Слайд 13Слайд 14Описание слайда:
Первичный и вторичный остеоартроз Остеохондроз позвоночника (спондилоартроз) Другие дегенеративно-дистрофические заболевания позвоночника (грыжи и протрузии дисков) Травмы суставов и позвоночника
Слайд 15Слайд 16Слайд 17Описание слайда:
Состав Терафлекс Адванс Терафлекс Адванс №60, №100 В 1 капсуле: Хондроитина сульфат 200 мг Глюкозамина сульфат 250 мг Ибупрофен 100 мг Показания: лечение болевого синдрома в фазе обострения при первичном и вторичном остеоартрозе суставов конечностей и межпозвонковых дисков. Приём по 2 капс. 2-3 раза в день, без консультации врача – не более 3 недель. Далее согласовать с врачом.
Слайд 18Описание слайда:
Состав Терафлекса Терафлекс №30, №60, №100 В 1 капсуле: Хондроитина сульфат 400 мг Глюкозамина гидрохлорид 500 мг Показания: Дегенеративно-дистрофические заболевания суставов и позвоночника: остеоартоз I – III стадии, первичный и вторичный остеоартроз, остеохондроз Приём по1 капс. 3раза в день 3 недели, затем 2 раза в день, курс 3-4 мес.
Слайд 19Описание слайда:
Состав Терафлекс М крем Хондроитина сульфат 0,8 % Глюкозамина гидрохлорид 0,3% Камфора 3,2% Масло мяты перечной 0,9% Показания: Дегенеративно-дистрофические заболевания суставов и позвоночника (в том числе остеоартроз и остеохондроз). Крем наносят полоской 0,5 -1 см и втирают. Эффект устойчивый чере 3-4 недели.
Слайд 20Описание слайда:
Результаты экспериментальных исследований Под воздействием медикаментозной терапии препаратами ГАГ (глюкозамин + хондроитин) объективно увеличивается количество и размеры хондроцитов на единицу площади суставного хряща.
Наиболее эффективно восстановление происходило в группе животных, где моделировались переломы с незначительной площадью повреждения суставного хряща.
Наибольшие дистрофические изменения в хряще наблюдали после моделирования переломов со значительной площадью повреждения суставного хряща без дополнительной стимуляции репаративной регенерации ГАГ.
Слайд 21Описание слайда:
Электронномикроскопическое исследование хондроцитов
Слайд 22Слайд 23Описание слайда:
Световая микроскопия хряща
Слайд 24Описание слайда:
АЛФЛУТОП Инъекционный хондропротектор В 1 мл – 0.01 г содержится стандартизированный очищенный (обезжиренный и депротеинизированный) экстракт из 4-х видов морских рыб
Слайд 25Описание слайда:
Уникальные преимущества Алфлутопа Алфлутоп проявляет свое действие на 1-2-й неделе от начала терапии ( в зависимости от способа введения). Длительность полного курса терапии 20 дней, 34 дня (в зависимости от способа введения) Алфлутоп — препарат с комплексным составом, сходным с матриксом гиалинового хряща. Алфлутоп оказыает защитное влияние на слизистую оболочку ЖКТ
Слайд 26Описание слайда:
Алфлутоп представляет собой естественный компонент хрящевого матрикса
Слайд 27Описание слайда:
Хондроитин
Слайд 28Описание слайда:
Гиалуроновая кислота
Слайд 29Описание слайда:
Кератансульфат
Слайд 30Слайд 31Описание слайда:
Многокомпонентный механизм действия АЛФЛУТОПА
Слайд 32Описание слайда:
Дополнительные эффекты Алфлутопа Антиоксидантная активность Гастропротективное действие Угнетение фактора ангиогенеза
Слайд 33Описание слайда:
Гастропротективный эффект «Алфлутоп повышает эффективность стандартной противоязвенной терапии (укорачивает сроки эпителизации язв и эрозий ЖКТ, возникших при приеме НПВС)»
Слайд 34Описание слайда:
АЛФЛУТОП
ПОКАЗАНИЯ К ПРИМЕНЕНИЮ Остеоартроз Остеохондроз Спондилез Травматические дистозы Периартрит Фибромиалгия Восстановительный период после оперативных вмешательств на опорно-двигательном аппарате Дегенеративно-дистрофические поражения суставов на фоне метаболических остеопатий
Слайд 35Описание слайда:
Схемы назначения
АЛФЛУТОПА
Слайд 36Слайд 37Слайд 38Слайд 39Описание слайда:
ОСНОВНЫЕ ПРЕИМУЩЕСТВА АФЛУТОПА Натуральный препарат; По комплексному составу сходен с матриксом гиалинового хряща; Высокая эффективность подтверждена результатами многочисленных клинических исследований; Снижение терапевтической дозы одновременно принимаемых НПВС на 60-90%; Замена местного введения кортикостероидов; Возможность применения у пациентов с желудочно-кишечными и сердечно-сосудистыми заболеваниями.
Слайд 40Описание слайда:
Внутрисуставное введение препаратов гиалуроновой кислоты. Показание : ОА I-III степени в отсутствии синовита. Препараты гиалуроновой кислоты (синвиск, ферматрон, гиалган, гиалуронан, остенил) или ее дериваты (гилан) вводятся внутрисуставно, обычно раз в неделю, на курс 3-5 инъекций по 2 мл. Продолжительность действия 1-3 недели, до нескольких месяцев. Повторять курсы – 1раз в 6 месяцев.
Слайд 41Слайд 42Слайд 43Слайд 44Слайд 45Слайд 46
Источник: https://myslide.ru/presentation/skachat-xondroprotektory
Лечение артроза крупных суставов препаратом Остеомед
Авторы: Раскачкин В.А., Токарев А.В., Панов И.В.
Центр спортивной медицины «Бароком»,
ГБУЗ «Городская поликлиника» поликлиника № 9
Применение биологически активного препарата «Остеомед» в комплексном лечении артрозов крупных суставов
История вопроса и актуальность проблемы
Согласно данным демографических исследований последних лет, населения Земли постепенно стареет. К концу 2014 года на планете насчитывалось почти 600 миллионов человек в возрасте старше 60 лет, по прогнозам к 2050 г. их станет 2 млрд.
, что составит 22% всего населения.
Общее «старение» населения планеты влечет за собой изменение структуры фоновых болезненных состояний, а именно — рост удельного веса инволюционных дегенеративных процессов, среди которых наиболее серьезную проблему представляет остеоартроз.
Остеоартроз (ОА) (по международной классификации остеоартрит) — хроническое прогрессирующее заболевание суставов, характерным признаком которого является появление деструктивных изменений в суставных хрящах и субхондральных отделах костей. В патологический процесс вовлекаются также околосуставные мышцы и связки, капсулы сустава, синовиальные оболочки.
Остеоартроз представляет собой достаточно широко распространенное заболевание суставов, часто являющееся причиной временной и стойкой утраты трудоспособности. Согласно эпидемиологическим исследованиям, 10 — 12% населения страдают остеоартрозом (Астапенко М.Г., 1977).
Эпидемиологическое изучение гонартроза в США показало, что у половины населения имеется риск заболевания остеоартрозом. Среди больных преобладают лица старше 65 лет, женщины страдают этим заболеванием чаще, чем мужчины.
Необходимость усиленного внимания к проблемам, связанным с остеоартрозом, определяется его социальным значением, так как в течение нескольких последних десятилетий число случаев временной и стойкой нетрудоспособности по этой причине увеличилась в 3-5 раз.
Остеоартроз является наиболее распространенным хроническим заболеванием суставов. Остеоартроз, как правило, наиболее часто развивается в коленных и тазобедренных суставах.
Основным патофизиологическим фактором остеоартроза является недостаточность процессов репарации поврежденного хряща, и, по данным последних исследований, свидетельствуют о дополнительной и интегральной роли костной и синовиальной ткани.
Образование остеофитов, субхондральный склероз и истертость суставных поверхностей являются важными признаками в лучевой диагностике заболевания. Основными симптомами при остеоартрозе являются: боль, ограничение движения и хруст, утренняя скованность.
Остеоартрит снижает качество жизни больных в большей степени, чем заболевания внутренних органов и является одной из основных причин ограничения функциональных возможностей пациентов [1,4,5].
Согласно национальным и международным рекомендациям, в лечении остеоартрита основное значение имеют: обучение больных, контроль веса, физические упражнения, ортопедические мероприятия (применение артезов, стелек с приподнятым латеральным краем и т.д.
), назначение ненаркотических анальгетиков, трамадола, нестероидных противовоспалительных препаратов, а также препаратов хондроитина и глюкозамина, антидепрессантов, внутрисуставное введение глюкокортикостероидов.
Основным недостатком лекарственной терапии является наличие различных побочных эффектов от вводимых препаратов, что ограничивает их длительное применение и делает актуальным поиск эффективных и безопасных методов коррекции терапии ОА. Значимое место в лечении ОА принадлежит лечебным физическим факторам, использование которых потенциирует действие лекарственных средств, уменьшает симптомы и тормозит прогрессирование заболевания.
Благодаря новейшим достижениям в изучении патогенеза ОА наметился определенный прогресс в лечении заболевания.
Терапия ОА, назначенная на ранних стадиях патологического процесса, должна быть направлена на решение следующих задач: уменьшение боли и воспаления, снижение частоты обострений и поражения новых суставов, замедление прогрессирования и предотвращение инвалидности, улучшение качества жизни больного. [6]
Экпериментальные исследования подтвердили значение локальных травмирующих воздействий и местной тканевой гипоксии в патогенезе деформирующего артроза коленного сустава и установили, что внутрисуставная оксигенация оптимизирует кровообращение и репаративную регенерацию, нормализует окислительный метаболизм в травмированных тканях. Внутрисуставная оксигенация предупреждает развитие склероза синовиальной оболочки, жировых тел, внутрисумочных спаек, предупреждает или прерывает прогрессирование дегенеративно-дистрофического процесса в суставном хряще. [1,2,3]
Неингаляционная оксигенотерапия — это старый незаслуженно забытый метод, однако новые экспериментальные и клинические наблюдения дают более широкое представление о патогенетическом действии кислорода как в области местного введения, так и на весь организм. С 1983 г.
в травматологии и хирургии начала широко применяться неингаляционная оксигенотерапия при заболеваниях и травмах опорно-двигательного аппарата, так метод сочетанного применения локальной баротерапии с параартикулярным введением кислорода у больных с деформирующим артрозом нижних конечностей активно использовался в Центральной городской больнице им.Г.А. Захарьина в г. Пензе. (Рационализаторское предложение №34 от 26.06.1987, А.И. Сафронов, В.А. Раскачкин, «Метод сочетанного применения локальной баротерапии с параартикулярным введением кислорода больным с деформирующим артрозом нижних конечностей».
В процессе проведения данного исследования авторами оценивалась возможность применения метода «вакуум-компрессорной» терапии в сочетании с традиционными методами при лечении гонартрозов.
Целью проводимых лечебных воздействий являлось устранение местной гипоксии и стимулирование интенсификации метаболизма пораженных тканей, снижение микроциркуляторного застоя в них за счет создания пассивной гиперемии и усиления дополнительного коллатерального кровотока (Полякова Л.В. И др., 2008).
Сеансы баровоздействий на поврежденные конечности производились с помощью барокамеры активной гиперемии (БАГ). Использование «вакуум-компрессорной» терапии в условиях барокамеры активной гиперемии в сочетании с традиционными методами лечения достоверно улучшает результаты лечения гонартрозов.
К препаратам, способным не только уменьшить болевой синдром, но и, возможно замедлить прогрессирование ОА, относится биологически активный препарат «Остеомед», разработанный и выпускаемый Пензенским предприятием «Парафарм».
В состав препарата входят: цитрат кальция 200 мг., рибофлавина гидрохлорид (В6) 0,3 мг., гомогенат трутневого расплода (перетертые личинки трутней) 100 мг.
Трутневый расплод является донатором гормонов эстрадиола, пролактина, тестостерона, прогестерона и многих других полезных веществ. [7,8]
В доступной литературе мы не обнаружили сведений о количественной и качественной оценке эффективности препарата «ОСТЕОМЕД» в сочетании с традиционными методами лечения и параартикулярным введением озона при поражениях крупных суставов (гонартрозах). Указанное обстоятельство и вышеприведенные сведения о свойствах препарата «ОСТЕОМЕД» явились основанием для выполнения данного исследования.
Цель работы
Изучение эффективности препарата «Остеомед» в комплексном лечении артроза.
Материалы и методы исследования
Исследование проводилось на базе лаборатории спортивной медицины «БАРОКОМ» (г. Пенза) и городской поликлиники №9 г. Пензы.
Обязательным условием проведения исследований являлось соблюдение идентичности условий проведения процедур, приема препаратов и обследований.
В исследовании приняли участие 90 мужчин и женщин в возрасте от 40 до 70 лет, страдающих остеоартрозом коленных и тазобедренных суставов. Все они, в случайном порядке, были распределены на три группы.
В I группу вошли 22 женщины и 8 мужчин в возрасте от 40 до 70 лет с продолжительностью заболевания от 8 до 60 месяцев. Двадцати двум больным был выставлен диагноз двухсторонний гонартроз (ГА).
Причем, тяжесть заболевания характеризовалась II степенью заболевания. Увеличение объема мягких тканей в области пораженных суставов при первичном измерении составляло от 1,3 до 3 см.
Во II группу вошли 30 больных, (26 женщин и 4 мужчин) в возрасте от 40-70 лет. У 18 из них была обнаружена 2-я стадия гонартроза, а у 20- 2-х сторонний гонартроз. Увеличение объема мягких тканей в области пораженных суставов составило от 1,3 до 3,1 см.
В III группу вошли 30 человек: 23 женщины, 7 мужчин в возрасте от 40 до 70 лет. У 19 человек данной группы была выявлена вторая стадия гонартроза, 25 человек — страдали 2-х сторонним гонартрозом. Увеличение объема мягких тканей в области пораженных суставов составляло от 1,2 до 3,2 см.
Для измерения биомеханических параметров нижних конечностей в качестве информативных критериев состояния больных использовались данные, полученные с помощью прибора гониометр (Авторское свидетельство № 1301379, заявка № 3947938. Приоритет от 19.08.85г.
, зарегистрированное в Государственном реестре изобретений СССР 8 декабря 1986 года, авторы Раскачкин Владимир Алексеевич, Каушлы Ким Мустафович, Цодыкс Владимир Моисеевич). Гониометр — это устройство (приложение, рисунок 5), предназначенное для измерения биомеханических параметров нижней конечности человека.
Оно определяет различные виды деформации голени и стопы и дает этим показателям количественную оценку.
Гониометр позволяет измерить практически все виды деформаций голени и стопы и дает возможность провести сравнительный анализ здоровой и пораженной конечностей, выработать на основе полученной информации тактику ликвидации деформаций, что позволяет с меньшей травматичностью и более быстро провести коррекцию деформаций. В нашем исследовании определялись следующие показатели: углы сгибания и разгибания в суставах до и после проведения курса лечения в группах.
В базовый лечебный комплекс, применявшийся в лечении больных всех групп, вошли нестероидные противовоспалительные препараты, хондропротекторы, физиотерапевтические процедуры.
Кроме того, больным II и III групп местно в область пораженных суставов параартикулярно водился О 3 по 5-10 см3 два раза в неделю на протяжении 30 дней.
А больные III группы принимали препарат «ОСТЕОМЕД» по 2 таблетки 3 раза в день на протяжении месяца.
- Во время исследования нами определялись следующие величины:
- Показатели психоэмоционального статуса больных (по данным методики «САН» — самочувствие, активность, настроение)
- Показатель болевых ощущений – интенсивность боли (ИБ), определяемый в баллах (по 10-балльной шкале)
- Показатель объема мягких тканей (ОМТ), он измерялся сантиметровой лентой в области пораженных суставов
- Показатели угловых размеров при разгибании (УР) и сгибании (УС) суставов. Измерения проводились с помощью гониометра
- Определение показателей проводилось до и после проведения лечения в группах в одинаковых для всех участников условиях.
Статистическая обработка полученных данных проводилась с тиспользованием пакета прикладных программ «Statistica 10.0» для «Windows».
Определялись: средние значения, мода, медиана, стандартные отклонения, средняя квадратная ошибка, средняя ошибка средней, характер распределения.
Достоверность разности средних значений показателей рассчитывалась с помощью t-критерия Стьюдента для несвязанных выборок. Табличные данные представлены в виде среднего арифметического значения и величины средней ошибки средней x±m.
Результаты исследования и их обсуждение
На первом этапе анализировались результаты комплексного обследования по принятым в работе показателям.
Было отмечено отсутствие значимых различий средних значений показателей выраженности болевых ощущений, объема мягких тканей в области пораженных суставов, угловых размеров при сгибании и разгибании у пациентов трех выделенных групп во время первоначальных обследований. Состояние психоэмоционального статуса больных I, II и III групп по данным показателей самочувствия, активности и настроения методики «САН» было однотипным.
Второй этап исследований был посвящен определению динамики принятых в работе показателей в группах больных, получавших базовый лечебный комплекс (группа I), базовый лечебный комплекс и инъекции озона (группа II), а также – базовый лечебный комплекс, инъекции озона и курсовое лечение препаратом «ОСТЕОМЕД» (группа III).
Изменения показателей интенсивности болевых ощущений на протяжении первых двух недель лечения представлены в таблице №4.
Примечание: * — достоверность различий показателей между группами при p
Источник: https://osteomed.su/lecheniye-artroza-krupnykh-sustavov-preparatom-osteomed/
Этиология и лечение посттравматического остеоартроза
Одной из вариаций дегенеративно-дистрофических патологий сустава выступает посттравматический остеоартроз.
Зачастую он развивается на фоне переломов или после оперативного вмешательства в подвижное сочленение. Заболевание сопровождается болевым синдромом и приводит к потере двигательной функции.
В большинстве случаев посттравматический артроз лечат консервативно, хирургия применяется редко.
Этиология и патогенез
Посттравматическим остеоартрозом называется воспаление сустава, которое развилось на фоне травмы или длительной неподвижности.
Патология выражается постепенным разрушением хрящевой прослойки подвижного сочленения.
Уменьшение толщины или отсутствие хряща нарушает целостность и амортизацию сустава, кости, подстраиваясь под нарастающее давление, трутся друг об друга и смещаются.
Принято считать, что артрозу подвержены люди преклонного возраста, однако случаи посттравматического остеоартроза встречаются нередко у всех возрастных групп. Выделяют такие причины развития заболевания:
- перелом;
- разрыв капсульно-связочного аппарата;
- повреждение сухожилий;
- рубцевание тканей после операции.
Как проявляется?
Симптоматика деформирующего остеоартроза зависит от локализации заболевания, что отображено в таблице:
| Коленный | Отек |
| Нарушение двигательной функции | |
| Боль, которая усиливается ночью | |
| Хруст при движении | |
| Голеностопный | Снижение мышечного тонуса |
| Выраженный болевой синдром | |
| Нарушение походки | |
| Тазобедренный | Хромота |
| Атрофия мышц | |
| Плечевой | Невозможность поднять руку выше горизонтального положения |
| Трудности со сгибанием и разгибанием сустава | |
| Ноющая боль в плече или лопатке |
Интенсивность симптомов коррелируется степенью развития заболевания, выделяют три стадии артроза:
Вначале развития патологии человек может замечать легкую утреннюю скованность в сочленении.
- Первая. Пациент ощущает небольшой дискомфорт в подвижном сочленении. Артроз коленного сустава проявляется скованностью по утрам, которая проходит в течение получаса. Как правило, проявления мало выражены и не доставляют беспокойства больному.
- Вторая. Процесс разрушения хрящевой ткани ощутим и сопровождается интенсивным болевым синдромом. Нарушается двигательная функция сустава.
- Третья. Резко ограничивается подвижность поврежденного сустава. Болевой синдром невозможно снять обычными препаратами. Стадии характерно очень тяжелое состояние пациента.
Диагностические процедуры
Выявить ДОА можно, посетив хирурга, ортопеда или травматолога. Врач соберет анамнез, проанализирует жалобы и проведет клинический осмотр. Диагностировать деформирующий остеоартроз возможно методом пальпации, однако для уточнения нюансов заболевания назначают ряд инструментальных анализов:
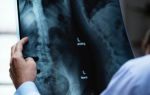
- Рентген. Исследование обнаружит нарушение целостности костей, наличие костных разрастаний, и определит стадию артроза.
- УЗИ. Оценивает состояние мягких тканей и сосудистую проходимость.
- КТ и МРТ. Компьютерные методы диагностики, которые считаются наиболее информативными, поскольку позволяют сделать серию подробных послойных снимков больного сустава.
- Артроскопию. Эта диагностически-лечебная операция проводится в случае неэффективности других методов диагностики.
Лечение деформирующего остеоартроза
Терапия ДОА всегда подразумевает комплексный подход.
Лечение болезни обязательно включает прием препаратов.
Схему лечебных мероприятий составляет врач на основании данных, полученных при исследованиях. Пациенту необходимо помнить, что артроз не допускает самолечения, для успешного исхода нужно четко следовать указаниям доктора.
Как правило, терапия включает такие мероприятия: прием лекарств, физиотерапевтические процедуры, санаторно-курортное лечение и профилактику. Третья степень артроза не поддается консервативным методам, применяют хирургию.
Какие лекарства назначают?
Деформирующий артроз лечат такими группами препаратов:
- Нестероидные противовоспалительные. Медикаменты снимают отечность, снижают болевой синдром и успешно купируют воспалительный процесс: «Диклак», «Вольтарен», «Нурофен».
- Глюкокортикостероиды. Применяют при неэффективности остальных методов или в случае присоединения инфекционного агента к воспалению: «Дексаметазон», «Кеналог», «Дипроспан».
- Обезболивающие. Снимают болевой синдром: «Анальгин», «Парацетамол». При интенсивных болях назначают наркотические рецептурные препараты.
- Хондропротекторы. Медикаменты нацелены на генерацию и восстановление суставного хряща: «Хондроксид», «Терафлекс».
- Витаминно-минеральные комплексы. Профилактические препараты с высоким содержанием кальция и витамина D.
Хирургическое лечение
С помощью артродеза можно устранить проблему, но двигательная функция сочленения будет утеряна.
Операция при артрозе применяется, когда традиционная терапия не результативна. Пациенту могут провести артродез. Это процедура, при которой удаляется поврежденный сустав, а кости соединяются друг с другом. Метод позволяет остановить процесс деформации, но сильно ограничивает двигательную функцию. Более современным и эффективным видом оперативного лечения выступает эндопротезирование. Метод позволяет заменить поврежденный сустав или его часть протезом.
Профилактика посттравматического остеоартроза
Основным условием предотвращения посттравматического артроза является своевременная диагностика и лечение травм.
Кроме того, следует придерживаться принципов здорового образа жизни: правильно питаться, соблюдать режим, высыпаться и равномерно распределять нагрузку.
Особое внимание следует уделить спорту: регулярные занятия физкультурой помогут держать в форме тело, разовьют ловкость и реакцию.
Источник: https://OsteoKeen.ru/oar/posttravmaticheskij-osteoartroz.html
Артроз посттравматический — причины и лечение
Один из критериев жизни – это движение, однако чем интенсивнее двигательная активность человека, тем быстрее изнашиваются его суставы, что приводит к естественному процессу возникновения деформирующего остеоартроза. Другой важной причиной артроза является получение травм при движениях, тогда врачи говорят о диагнозе «посттравматический артроз».
Причины возникновения посттравматического артроза
Медицинская наука выделяет две формы артроза, исходя из причин, вызвавших его: первичный и вторичный. Если к первичному остеоартрозу много вопросов, что стало причиной болезни, то вторичная форма чаще всего является следствием травмы.
Посттравматическому артрозу могут предшествовать растяжения, ушибы, подвывихи и другие травмы тканей и костей:
- сильные растяжения связочного аппарата;
- травмы прилегающих к суставу мышечных тканей;
- переломы с воспалительными процессами;
- нарушения метаболического процесса;
- проблемы эндокринной системы;
- повреждения мениска;
- инфекционные болезни, провоцирующие воспаление.
Таким образом, посттравматический артроз «получить» не так-то сложно, но в группу риска входят, в первую очередь, профессиональные спортсмены, у которых риск получения травмы намного выше среднестатистического человека.
Пожилые люди так же на порядок чаще страдают артрозом: не менее 60% людей от 60 лет и старше имеют диагноз «остеоартроз» той или иной стадии.
Между прочим, среди старшего населения чаще подвержены риску травмирования, растяжения, поскольку кальция в костях с возрастом становится меньше, связки – слабее, а организм уже не такой выносливый, что приводит к долгому заживлению переломов.
Всё это пагубно сказывается на здоровье суставов и хрящевой ткани.
Помимо этого, стоит сказать, что с возрастом, как и многие другие системы и органы человека, ухудшается качество синовиальной жидкости, которая служит для нормального вращения суставов, чтобы трение не вызывало болей, преждевременного износа хряща, субхондральной кости. Воспаления, вызванные травмами, будут провоцировать посттравматический артроз.
Степени посттравматического остеоартроза
Начальная, первая степень посттравматического артроза не отличается выраженной симптоматикой. Её проявления не особо заметны, изредка возникает дискомфорт после долгой ходьбы или с утра возникает скованность в движениях конечностей.
Надо сказать, что посттравматический артроз чаще всего поражает коленный, локтевой суставы, реже – голеностоп, плечи, тазобедренный сустав. Именно на первой стадии недуга легче всего побороть артроз.
К сожалению, обычно его замечают случайно при прохождении рентгенологического обследования, которое может выявить сужение межсуставной щели.
Вторая степень характеризуется значительным сужением межсуставного пространства, возможно появление мелких остеофитов. Человеку тяжело совершать привычные движения больными суставами.
Если речь идет о гонартрозе, голеностопном артрозе или коксартрозе, то становятся испытанием подъемы-спуски по лестнице.
Если говорить, об артрозе фасеточных суставов позвоночного столба – спондилоартрозе, то любые наклоны туловищем, шеей причиняют боль.
Трудность сгибания межпозвонковых дисков приводит к атрофии мышц шеи, спины, что еще больше усугубляет картину посттравматического артроза. Третья стадия условно определяется сильными, постоянными болями в пораженных суставах, почти их полным обездвижением. Рентген выявляет большое количество костных образований по краям суставов – остеофитов, почти полное отсутствие щели между суставами.
Лечение посттравматического артроза
Борьба за сустав принципиально не отличается при посттравматическом артрозе от остеоартроза иной этиологии. Главным здесь будет соблюдение комплексного лечения:
- медикаментозное лечение для подавления симптомов артроза;
- физиотерапевтические приемы и процедуры для нормализации обменных процессов, снятия воспалений, лучшего усваивания таблеток и мазей;
- средства народной медицины для снятия болей, насыщения организма витаминами, микроэлементами, полезными веществами;
- сеансы массажа для укрепления мышечного корсета;
- лечебная физкультура для повышения подвижности суставов, недопущения атрофии мышц, снижении нагрузки на суставы;
- прием хондропротекторов, подпитывающих хрящевую ткань;
- в самых тяжелых случаях – хирургическое вмешательство, включающее эндопротезирование (замена) больного сустава, операционное исправление деформаций, коррекция оси костей.
Полезным будет посещение санаториев, где будет возможность пройти процедуры грязевых ванн. Во время лечения посттравматического артроза нужно отказаться от занятия спорта с чрезмерной нагрузкой на суставы – футбол, скалолазание, хоккей, волейбол, теннис. Однако разрешается посещать бассейн – плавание положительно сказывается для разгрузки суставов, а также укрепляет мышцы. Вместо бега стоит предпочесть пешие прогулки.
Нельзя не сказать, что процесс излечения – дело не одного месяца и даже не одного года, если посттравматический артроз находится на 2-3 стадии. Поэтому стоит настроиться на упорную работу по спасению суставов. Чтобы не допускать деформирующего посттравматического артроза, следует избегать травм.
Ни одна травма не проходит бесследно. Рацион человека должен быть сбалансирован, вес – в норме, чтобы не было гнетущего давления на нижние конечности. В питании важно получать должное количество витаминов, минералов, элементов.
Для профилактики следует употреблять холодцы, желеобразные блюда, укрепляющие хрящ, связочный аппарат.
Источник: http://pro-artroz.ru/artroz/artroz-posttravmaticheskiy.html
Хондропротекторы в лечении остеоартроза | Лыгина | Современная ревматология
1.
Pelletier J.-P., Martel-Pelletier J., Abramson S.B. Osteoarthritis an inflammatory disease. Arthr Rheum 2001; 44(6): 1237—47.
Pincus T. Clinical evidence for osteoarthritis as an inflammatory disease. Curr Rheum Rep 2006; 3(6): 524—34.
Smith M.M., Ghosh P. Osteoarthritis: Current status and future directions. APLAR J Rheum 1998; 2: 27-53.
Lawrence R.C., Brummer Jm., Bier F. Osteoarthritis prevalence in the population and relationship between symptoms and x-ray changes. Ann Rheum Dis 1966; 25: 1—24.
Woolfe F.D., Pfleger B. Burden of major musculoskeletal conditions. Bull World Organ 2003; 81: 646—56.
Артеменко Н.А. Особенности прогрессирования и лечения остеоартроза. РМЖ 2005; 7(13): 403—6.
Алексеева Л.И., Цветкова Е.С. Остеоартроз: из прошлого в будущее. Науч.-практ. ревматология. 2009; 2 (прил.): 31—7.
Берглезов М.А., Андреева Т.М. Остеоартроз (этиология, патогенез). Вестн. травматол. и ортопед. 2006; 4: 79—86.
Верткин А.Л., Алексеева Л.И., Наумов А.В. и др. Остеоартроз в практике врача-терапевта. РМЖ 2008; 16(7): 476—80.
Артеменко Н.А., Чвамания М.А. Особенности прогрессирования и лечения остеоартроза. РМЖ 2005; 13(7): 403—7.
Бадокин В.В. Значение воспаления в развитии и течении остеоартроза. Cons med 2009; 11(9): 91—5.
Lippielo L., Grande D. In vitro chondroprotection of glucosamine and chondroitin sulfate in a rabbit model of a OA and demonstration of metabolic synergy on chondrocyte in vitro. Ann Rheum Dis 2000; 59(Suppl. 1): 266.
Teitelbaum S.L. Bone resorption by osteoclasts. Science 2000; 289: 147—8.
Henrotin Y., Reginster T. In vitro difference among nonsteroidal anti-inflammatory drug in their activities related to Osteoarthritis pathophysiology. Osteoarthr Cartil 1999; 7: 355—7.
Martel-Pelletier J., Pelletier J.-P. Inflammatory factors involved in Osteoarthritis. In: Osteoarthritis, Inflammation and Degradation: A Continuum. IOS Press, 2007; 3—13.
Connaghan P.G., Vanharanta H., Dieppe P.A. Is progressive osteoarthritis an atheromatous vascular disease? Ann Rheum Dis 2005; 64: 1539—41.
Маркин С.П. Остеоартроз: особенности диагностики и лечения. Cons med 2011; 13(9): 46—51.
Фоломеева О.М., Лебедева Л.С., Ушакова М.А. Инвалидность, обусловленная ревматическими заболеваниями, среди жителей Российской Федерации. Науч.-практич. ревматол. 2001; 1: 15.
Эрдес Ш.Ф., Фоломеева О.М. Ревматические заболевания и инвалидность взрослого населения Российской Федерации. Науч.-практич. ревматол. 2007; 4: 4—10.
Martel-Palletier J., Lajeunesse D., Palletier J.P. Etiopathogenesis of osteoarthritis. A textbook of reheumatology. Ed. By W.J. Koopman, L.W. Morelance. Baltimore: Lipencott, Willamse and Wilkins, 2005; 2199—226.
Heerdink E.R., Leufkens H.G., Herings R.M.C. et al. NSAIDs associated with increase risk of congestive heart in elderly patients taking diuretics. Arch Int Med 1998; 158: 1108—12.
Core M., Sadosky A., Tai K.-S. et al. Clinical comorbiditis, pain-related pharmacotherapy, and direct medical costs of patients with osteoarthritis in clinical practice. OA and Cartil 2010; 18(Suppl. 2), (abstr.); 281: s126.
Рачин А.П. Доказательная фармакоаналитика терапии остеоартроза. Фарматека 2007; 19: 81—6.
Савенков М.П., Бродская С.А., Иванов С.Н. и др. Влияние нестероидных средств на антигипертензивный эффект ингибиторов АПФ. РМЖ 2003; 19: 1056—9.
Page J., Henry D. Consumption of NSAIDs and the development of congestive heart failure in elderly patients. Arch Int Med 2000; 160: 777—84.
Warksman J.C. Nonselective nonsteroidal anti-inflammatory drugs and cardiovascular risk: are they safe? Ann Rharmacother 2007; 41: 1163—73.
Jordan K.M., Arden N.K., Doherty M. et al. EULAR Recommendation 2003: an evidence based approach to the management of knee osteoarthritis: Report of a Task Force of the Standing Committee for international Clinical Studies including Therapeutic Trials (ESCISIT). Ann Rheum Dis 2003; 62: 1145—55.
Leeb B.F., Schweitzer H., Montag K. et al. A meta-analysis of chondroitin-sulfate in the treatment of osteoarthritis. J Rheum 2000; 27: 205—11.
Алексеева Л.И. Симптоматические препараты замедленного действия при лечении остеоартроза. Cons med 2009; 11(9): 100—4.
Насонова В.А., Насонов Е.Л. Рациональная фармакотерапия ревматических заболеваний. М.: Литтерра, 2003; 800.
Volpi N. Oral bioavailability of chondroitin sulfate (Chomdrosulf) and its constituents in healthy male volunteers. Osteoarthr Cartil 2002; 10(10): 768—77.
Новиков В.Е. Хондропротекторы. Обзоры по клин. фарм. лек. тер. 2010; 8(2): 41—7.
Hathcoock J.N., Shao A. Risk assessment for Glucosamine and Chondroitin sulfate. Regul Toxicol Pharmacol 2007; 47: 78—83.
Алексеева Л.И., Шарапова Е.П. Хондроитин сульфат в лечении остеоартроза. РМЖ 2009; 17(21): 1448—53.
Monfort J., Nacher M., Montell E. et al. Chondroitin sulfate and Hyaluronic acid inhibit stromelysin-1 synthesis in human osteoarthritis chondrocytes. Drugs Exp Clin Res 2005; 31: 71—6.
Caraglia M., Beninati S., Alessandro A. et al. Alternative therapy of earth elements increases the chondroprotective effects chon-droitin sulfate in mice. Exp Mol Med 2005; 37: 476—81.
Chan P.S., Caron J. P., Orth M.W. Shortterm gene expression changes in cartilage explants stimulated with interleukin beta glucosamine and chondroitin sulfate. J Rheum 2006; 33: 1329—40.
Holzmann J., Brandi N., Zemann A. et al. Assorted effects of TGF-beta and chondroitin sulfate on p38and ERK _ activation levels in human articular chondrocytes stimulated with LPS. Osteoarthr Cartil 2006; 14: 519—25.
Monfort J., Pellietier J.-P., Garcia-Giralt N. et al. Biochemical basis of the effect of chondroitin sulfate on osteoarthritis articular tissues. Ann Rheum Dis 2008; 67: 735—40.
Чичасова Н.В., Мендель О.И., Насонов Е.Л. Остеоартроз как общетерапевтическая проблема. РМЖ 2010; 18(11): 729—34.
Горячев Д.В. Место препаратов хондроитин сульфата в арсенале средств для лечения остеоартроза. РМЖ 2008; 16(10): 478—80.
Landmesser U., Dikalov S., Price S.R. et al. Oxidation of tetrahydrobiopterin leads to uncoupling of endothelial cell nitric oxide syntetase in hypertension. J Clin Invest 2003; 111: 1201—9.
Stroes E., De Bruin T., de Valk H. et al. NO activity in familial combined hyperlipidemia: potential role of cholesterol remmants. Cardiovasc Res 1997; 36: 445—52.
Аннефельд М. Новые данные о глюкозамине сульфате. Науч.-практ. ревматол. 2005; 4: 76—80.
Register J., Rovati L., Deroisy R. et al. Glucosamine sulfate slows — down osteoarthritis progressin in postmenopausal women: pooled analysis of two large, independent, randomized double-blind placebocontrolled, prospective 3-year trials. Ann Rheum Dis 2002; 61(Suppl. 1). THU 0196.
Bruyere O., Burlet N., Delmas P. et al. Evaluation of Symptomatic Slow-Acting Drugs in Osteoarthritis Using the GRADE System. BMC Musculoskelet Dis 2008; 16(9): 165.
McAlindon T.E., LaValley M.P., Gulin J.P. et al. Glucosamine and chondroitin for treatment of osteoarthritis: a systematic quality assessment and meta-analysis. JAMA 2000; 283: 1469—75.
Towbeed T.E., Maxwell L., Anastassiades T.P. et al. Glucosamine therapy for treating osteoarthritis. Cochrane Database Syst Rev 2005; 2: CD002946.
Herrero-Beaumont G., Ivorra J.A., Del Carmen Irabado M. et al. Glucosamine sulfate in the treatment of knee osteoarthritis symptoms: a randomized, double-blind, placebo-controlled study using acetaminophen as side comparator. Arthr Rheum 2007; 56: 555—67.
Pawelka K., Gatterova J., Olejarova M. et al. Glucosamine sulfate use and delay of progression of knee osteoarthritis: a 3 year, randomized, placebo-controlled, double-blind study. Arch Intern Med 2002; 162: 2113—23.
Reginster J.Y., Deroisy R., Rovati L.C. et al. Long-term effects of glucosamine sulphate on osteoarthritisprogression: a randomized, placebo-controlled clinical trial. Lancet 2001; 27: 251—6.
Poolsup N., Suthisisang C., Channark P. et al. Glucosamine long-term treatment and the progression of knee osteoarthritis: systematic review of randomized controlled trials. Ann Pharmacother 2005; 39: 1080—7.
Leeb B.F., Schweitzer H., Montag K. et al. A meta-analysis of chondroitinsulfate in the treatment of osteoarthritis. Osteoar Cartil 1999; 7(Suppl. A): abstr. 130.
Bana G., Jamard B., Verrouil E. et al. Chondroitin sulfate in the management of hip and knee OA: an overview. Adv Pharmacol 2006; 53: 507—22.
Michel B.A., Stucki G., Frey D. et al. Chondroitin 4 and 6 sulfatein osteoarthritis of the knee: A randomized, controlled trial. Arthr Rheum 2005; 52(3): 779—86.
Verbuggen G., Goemaere S., Veys E.M. Chondroitin sulfate: S/DMOAD (structure/disease modifying antiosteoarthritis drug) in the treatment of finger joint OA. Osteoarthr Cartil 1998; 6 (Suppl. A): 37—8.
Rovetta G., Monteforte P., Molfetta G. et al. A two-years study of chondroitin sulfatein erosive osteoarthritis of the band: behavior of erosions, osteophytes, pain and hand dysfunction. Drug Exp Clin Res 2004; 30(1): 11—6.
Алексеева Л.И., Чичасова Н.В., Беневоленская Л.И. и др. Перспективы комбинированной хондропротективной терапии остеоартроза. Результаты открытого рандомизированного исследования препарата Артра у больных гонартрозом. Науч.-практ. ревматология 2004; 4: 77—9.
Лила А.М., Мазуров В.И., Шидловская О.В. и др. Терафлекс в комплексной терапии остеоартроза коленных суставов и остеохондроза позвоночника. РМЖ 2005; 13(24): 1618—22.
Чичасова Н.В., Алексеева Л.И., Беневоленская Л.И. и др. Новое направление в лечении остеоартроза — комбинированная терапия хондроитин сульфатом и глюкозамина гидрохлоридом. РМЖ 2004; 12(23): 1337—41.
Clegg D.O., Reda D.J., Harris C.L. et al. Glucosamine, chondroitin sulfate, and the two in combination for painful knee osteoarthritis. N Engl J Med 2006; 354(8): 795—808.
Fidelix T.S.A., Soares B.G.D.O., Trevisani V.F.M. Diacerein for osteoarthritis. The Cochrane Database of Systematic Reviews 2006.
Источник: https://mrj.ima-press.net/mrj/article/view/414
Способ лечения посттравматического деформирующего остеоартроза
Изобретение относится к медицине, а именно к ортопедии, и может быть использовано для лечения дегенеративно-дистрофических заболеваний суставов, в частности посттравматического деформирующего остеоартроза.
Осуществляют воздействие общими радоновыми ваннами с концентрацией радона 0,2 кБк/л экспозицией 15 минут, температурой 36°С на курс 10 процедур, проводимых через день. В свободные от радонотерапии дни воздействуют пелоидотерапией при температуре 20-24°С, экспозиция 20 минут, на курс 10 процедур через день.
Ежедневно проводят низкочастотную магнитотерапию переменным магнитным полем с частотой 50 Гц, магнитной индукцией 25-30 мТл, на курс 20 ежедневных процедур по 15 минут. Местно осуществляют наложение альфа-аппликатора с дочерними продуктами радона с удельной активностью 37 Бк/см2, экспозиция 120 минут, на курс 20 ежедневных процедур.
Внутрисуставное введение препарата «Алфлутоп» по 2 мл осуществляют с интервалом 3 дня, на курс 5 процедур. Способ технически прост, высокоэффективен, обеспечивает, в том числе, увеличение толщины суставного гиалинового хряща. 2 ил.
Изобретение относится к медицине, а именно к ортопедии, и может быть использовано для лечения дегенеративно-дистрофических заболеваний суставов, в частности посттравматического деформирующего остеоартроза.
Известно, что механическое повреждение и последующее реактивное воспаление в суставе ведут к нарушению метаболизма суставного гиалинового хряща, появлению в нем трещин, участков разволокнения и фрагментации, при этом дегенеративно-дистрофические изменения приобретают характер хронического самоподдерживающегося процесса, приводят к формированию дефектов суставного хряща различной глубины и площади. В этих ситуациях вследствие низкой репаративной способности гиалинового хряща на наиболее нагружаемых участках суставных поверхностей сустава в течение 3-5 лет развивается деформирующий остеоартроз, характеризующийся прогрессирующей дегенерацией хряща в виде уменьшения его толщины. Основной целью лечения этой категории больных является стабилизация дегенеративно-дистрофического процесса в суставе, одним из основных показателей которой является сохранение толщины и структуры суставного гиалинового хряща. Указанная цель в большинстве случаев реализуется путем назначения базисной медикаментозной терапии в виде длительного приема пероральных или парентеральных форм хондропротекторов. Возникающая при этом значительная лекарственная нагрузка нередко приводит к развитию побочных эффектов.
Известен способ лечения посттравматического деформирующего артроза, заключающийся в трансплантации пункционным методом аутогенных мезенхимальных стволовых клеток (МСК) в полость пораженного сустава [Kotobuki N.
, Hirose M., Takakura Y., Ohgushi H. Cultured autulogous human cells for hard tissue regeneration: preparation and characterization of mesenchymal stem cells from bone marrow // Artificial Organs, 2004. — 28(1). — P.
33-39].
Положительный результат отмечен через 1,5-2 месяца и проявляется в восстановлении дефектов суставного гиалинового хряща путем стимуляции его регенераторных возможностей. Однако применение стволовых клеток мало изучено, методика сложна, дорогостояща; занимает продолжительное время и не обеспечивает достаточного воздействия на патогенез посттравматического остеоартроза.
Наиболее близким по достигаемому положительному результату (прототипом) является способ лечения посттравматического деформирующего артроза путем введения в полость пораженного сустава хондропротекторов, которые стимулируют синтез мукополисахаридов и гиалуроновой кислоты, обеспечивая тем самым повышение синтеза компонентов хрящевого матрикса и торможение процессов деструкции хряща [И.Б.Героева, М.Б.Цыкунов. Консервативное лечение остеоартроза крупных суставов. Вестник травматологии и ортопедии — 1994 — №3. — С.51-56].
Недостатками известного способа являются малая эффективность вследствие одностороннего воздействия на систему жизнеобеспечения хряща; длительность курса лечения (от 2 до 4 месяцев) и травматичность из-за большого количества пункций сустава.
Авторы предлагают эффективный способ лечения посттравматического деформирующего остеоартроза, обеспечивающий регенерацию суставного гиалинового хряща путем стимуляции репаративного хондрогенеза.
Техническим результатом является повышение эффективности лечения.
Технический результат достигается тем, что с учетом основных патогенетических механизмов развития посттравматического деформирующего остеоартроза на пораженный сустав осуществляют сочетанное воздействие общей и местной радонотерапией, пелоидотерапией, низкочастотной переменной магнитотерапией, внутрисуставным введением хондропротектора «Алфлутоп». Используемые методы дополняют друг друга и усиливают эффект, который подтвержден ультразвуковым исследованием суставов.
Изобретательский уровень заключается в выборе таких лечебных мероприятий, которые подобраны в такой строгой последовательности, что позволяет получить положительный эффект при лечении посттравматического деформирующего остеоартроза без развития побочных эффектов.
Способ осуществляют строго поэтапно следующим образом.
В первой половине дня больные получают общие радоновые азотно-кремнистые ванны с концентрацией радона 0,2 кБк/л в температурном режиме 36°С с экспозицией 15 минут, на курс 10 процедур через день, эквивалентная доза составляет 220 мкЗв. В эти же часы через день с радонотерапией больным проводят пелоидотерапию в виде аппликаций иловой сульфидной грязи температурой 20-24°С на область пораженного сустава с экспозицией 20 минут, 10 процедур на курс.
Вторым этапом спустя 1-2 часа после радоно- или пелоидотерапии больные получают низкочастотную магнитотерапия переменным магнитным полем от аппарата «АМТ-75 — Полюс-2» с частотой 50 Гц и магнитной индукцией 25-30 мТл, на курс 20 ежедневных процедур продолжительностью 15 минут.
Третьим этапом сразу после магнитотерапии больным на пораженные суставы проводят местную накожную альфа-терапию. Для этого используют радоновый альфа-аппликатор удельной активностью 37 Бк/см2 с дочерними продуктами радона, заранее приготовленный в установке И.В.Малышева. Процедуры проводят ежедневно в течение 20 дней, экспозиция составляет 120 минут.
Четвертым этапом во второй половине дня больным выполняют внутрисуставные инъекции 2 мл препарата «Алфлутоп» (Биотехнос, Румыния), на курс 5 процедур с интервалом 3 дня.
Морфологическую оценку результатов лечения осуществляют посредством артросонографии до и после курса реабилитации на аппарате «SonoAce Medison — 8000» (Южная Корея) линейным датчиком 7,5 МГц путем количественной оценки толщины суставного гиалинового хряща на нагружаемых поверхностях медиальных мыщелков бедренных костей в положении больного лежа на спине. Увеличение толщины суставного хряща по окончании курса лечения расценивали как положительный структурно-модифицирующий эффект сочетанного применения общей и местной радонотерапии, пелоидотерапии, низкочастотной магнитотерапии переменным магнитным полем и внутрисуставного введения препарата «Алфлутоп».
Клинический пример.
Больная З., 39 лет, в 2006 году находилась на лечении в отделении реабилитации больных с заболеваниями опорно-двигательного аппарата санатория «Белокуриха» с диагнозом: двусторонний посттравматический гонартроз 1 стадии по Kellgren-Lowrence.
До начала лечения больной выполнена артросонография коленных суставов, которая позволила определить толщину суставного гиалинового хряща: в правом коленном суставе — 0,26 см, в левом 0,25 см.
Больной проведен курс лечения, включающий в себя сочетанное применение радоновых ванн, местной накожной терапии радоновым альфа-аппликатором с дочерними продуктами радона, пелоидотерапии, низкочастотной магнитотерапии переменным магнитным полем и внутрисуставным введением препарата «Алфлутоп».
По окончании курса лечения повторно выполнена артросонография: отмечено увеличение толщины суставного хряща в левом коленном суставе с 0,25 см до 0,28 см, в правом с 0,26 до 0,29 см.
На чертежах 1 и 2 представлены артросонограммы коленных суставов больной 3., 39 лет, на которых объективно зафиксирован положительный структурно-модифицирующий эффект, о чем свидетельствует увеличение толщины суставного гиалинового хряща после лечения.
Таким образом, способ лечения, включающий сочетанное применение общей и местной радонотерапии, пелоидотерапии, низкочастотной магнитотерапии переменным магнитным полем и внутрисуставное введение препарата «Алфлутоп», высокоэффективен, технически прост, занимает непродолжительное время и может широко применяться на бальнеологических радоновых курортах.
Способ лечения посттравматического деформирующего остеоартроза, заключающийся в применении хондропротектора, отличающийся тем, что дополнительно осуществляют поэтапное сочетанное воздействие общими радоновыми ваннами с концентрацией радона 0,2 кБк/л экспозицией 15 мин, температурой 36°С эквивалентной дозой 220 мкЗв, на курс 10 процедур через день; пелоидотерапией температура 20-24°С, экспозиция 20 минут 10 процедур через день с радонотерапией; низкочастотной магнитотерапией переменным магнитным полем с частотой 50 Гц, магнитной индукцией 25-30 мТл, на курс 20 ежедневных процедур по 15 мин; местной накожной терапией альфа-аппликатором с дочерними продуктами радона с удельной активностью 37 Бк/см2, экспозиция 120 мин, на курс 20 ежедневных процедур, причем в качестве хондропротектора применяют препарат «Алфлутоп» внутрисуставным введением по 2 мл с интервалом 3 дня, на курс 5 процедур.
Источник: https://findpatent.ru/patent/234/2342921.html
 Описание слайда:
Описание слайда: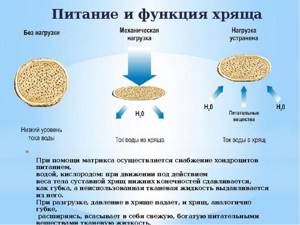 Описание слайда:
Описание слайда: Слайд 4
Слайд 4 Слайд 5
Слайд 5 Описание слайда:
Описание слайда: Слайд 7
Слайд 7 Описание слайда:
Описание слайда: Описание слайда:
Описание слайда: Описание слайда:
Описание слайда: Описание слайда:
Описание слайда: